Síndrome de Guillain-Barré durante la transmisión actual del virus del Zika, Puerto Rico, del 1 de enero al 31 de julio del 2016
Semanal / 2 de septiembre del 2016 / 65(34);910-914
Datos del artículo
Las vistas equivalen a las vistas de páginas más las descargas de PDFVistas:
Citas:
Métricas alternativas:
Detalles de la métricaEl 26 de agosto del 2016 se publicó este informe en línea como un adelanto del MMWR.
Emilio Dirlikov, PhD1,2; Chelsea G. Major, MPH3,4; Marrielle Mayshack1,4; Nicole Medina, MPH3; Desiree Matos3; Kyle R. Ryff, MPH1; Jomil Torres-Aponte, MS1; Rebecca Alkis5; Jorge Munoz-Jordan, PhD3; Candimar Colon-Sanchez, MS3; Jorge L. Salinas, MD2; Daniel M. Pastula, MD3,6; Myriam Garcia, MT7,8; Marangely Olivero Segarra, MS7,8; Graciela Malave, MT7,8; Dana L. Thomas, MD9; Gloria M. Rodríguez-Vega, MD10; Carlos A. Luciano, MD11; James Sejvar, MD12; Tyler M. Sharp, PhD3; Brenda Rivera-Garcia, DVM1 (ver las afiliaciones de los autores)
Ver la referencia bibliográfica sugeridaResumen
¿Qué se sabe sobre este tema?
El Síndrome de Guillain-Barré (SGB) es un trastorno autoinmune poco común caracterizado por una variación en el grado de debilidad, anomalías sensoriales, y disfunción de la autonomía debido a un daño del nervio periférico o en la raíz del nervio. Los países afectados por el virus del Zika han informado un incremento en las cifras de casos de SGB. Tras la identificación de la transmisión local del virus del Zika en Puerto Rico en diciembre del 2015, el Departamento de Salud de Puerto Rico implementó el Sistema de Vigilancia Pasiva de SGB en febrero del 2016.
¿Qué información agrega este informe?
Entre los 56 pacientes con presunto SGB que tuvieron aparición de síntomas neurológicos durante el 1 de enero y el 31 de julio del 2016, se halló la presencia de evidencia de Zika u otra infección por flavivirus en 34 (61%), incluidos 10 (18%) con infección confirmada por el virus del Zika. La media de la edad de los 34 pacientes fue de 55 años, y el 59% eran mujeres. Treinta (88%) pacientes informaron enfermedad aguda antes de desarrollar síntomas neurológicos, con un tiempo medio hasta la aparición de los síntomas neurológicos de 5 días. Un paciente murió a causa de un choque séptico después de un tratamiento de SGB. Además, se detectó que había evidencias del virus del Zika o de una infección por un flavivirus en siete pacientes con trastornos neurológicos que no eran por SGB.
¿Cuáles son las consecuencias para la práctica de salud pública?
Las personas con signos o síntomas que concuerden con el SGB deben buscar atención médica de inmediato. Los proveedores de atención médica que evalúan a pacientes con enfermedades neurológicas deben tener en cuenta al SGB e informar los casos presuntos a las autoridades de salud pública. Se recomienda a los residentes de Puerto Rico y a los que viajan a este país que sigan las recomendaciones existentes para la prevención de la infección por el virus del Zika.
El síndrome de Guillain-Barré (SGB) es un trastorno autoinmune postinfeccioso caracterizado por debilidad y flacidez bilateral en las extremidades, el cual es atribuible a daños en el nervio periférico (1). Se ha informado una mayor incidencia de SGB en países con transmisión local del virus del Zika; un flavivirus transmitido principalmente por ciertos mosquitos de la especie Aedes (2). En Puerto Rico, tres virus transmitidos por artrópodos (arbovirus) están en circulación actualmente: zika, dengue, y chikunguña. La primera infección por el virus del Zika contraída a nivel local en Puerto Rico fue informada en diciembre del 2015 (3). En febrero del 2016, el Departamento de Salud de Puerto Rico (PRDH), con la asistencia de los CDC, implementaron el Sistema de Vigilancia Pasiva de SGB (GBPSS) para identificar nuevos casos presuntos de SGB (4). Se identificaron cincuenta y seis presuntos casos de SGB con aparición de signos neurológicos durante el 1 de enero y el 31 de julio del 2016. Treinta y cuatro (61%) pacientes tenían evidencia de infección por el virus del Zika o de un flavivirus; la media en la edad de estos pacientes fue de 55 años (rango= 21–88 años), y 20 (59%) pacientes eran mujeres. Estos 34 pacientes eran residentes de siete de ocho regiones de salud pública del Departamento de Salud de Puerto Rico (PRHD, por sus siglas en inglés). Todos los 34 pacientes fueron hospitalizados y tratados con inmunoglubilina G intravenosa (IVIg); el tratamiento estándar para el SGB; 21 (62%) tuvieron que ser ingresados a unidades de cuidado intensivo, incluidos 12 (35%) que tuvieron que ser asistidos mediante entubación endotraqueal y ventilación mecánica. Un paciente murió de choque séptico después de un tratamiento de SGB. Además, 26 casos de afecciones neurológicas, que no eran SGB, fueron informados mediante el GBPSS, incluidos siete (27%) en pacientes con evidencia del virus del Zika o de infección por un flavivirus. Los residentes de Puerto Rico y los países con transmisión activa del virus del Zika y las personas que viajan allí deben seguir las recomendaciones para la prevención de infecciones del virus del Zika.* Las personas con signos o síntomas que concuerdan con el SGB deben buscar atención médica de inmediato. Los proveedores de atención médica en áreas con transmisión actual a nivel local que examinan pacientes con enfermedades neurológicas deben tener en cuenta al SGB e informar los casos presuntos a las autoridades de salud pública.
Vigilancia epidemiológica del SGB
En febrero del 2016, como parte de la respuesta actual a la transmisión local del virus del Zika (3–5), el Departamento de Salud de Puerto Rico implementó el Sistema de Vigilancia Pasiva de SGB (GBPSS) con asistencia de los CDC. Se les solicita a los proveedores de atención médica de toda la isla que informen todos los pacientes con presunto SGB al Departamento de Salud de Puerto Rico enviando un formulario de informe de caso† junto con los especímenes del paciente (suero, orina, líquido cefalorraquídeo [LCR], y saliva). También se los insta a que envíen los informes de los pacientes con otros trastornos neurológicos y presunta infección arboviral como antecedente. Todos los especímenes enviados son sometidos a pruebas en la División del Dengue de los CDC (San Juan, Puerto Rico) o en el Laboratorio de Emergencias Químicas y Biológicas del Departamento de Salud de Puerto Rico usando un ensayo de reacción en cadena de la polimerasa con transcripción inversa Trioplex (RT-PCR) para detectar ácido nucleico de los virus del Zika, dengue y chikunguña.§ También se realizan pruebas a los especímenes de suero y LCR mediante un ensayo de inmunoadsorción enzimática para inmunoglobulina M (IgM) (ELISA) para todos los tres virus. Se considera que las personas a las que la RT-PCR les detectó ácido nucleico del virus del Zika, en cualquier espécimen, tienen infección confirmada por el virus del Zika. Se considera que las personas con una RT-PCR con resultado negativo para el virus del Zika, en todos los espécimenes a los que se les realizaron las pruebas, tienen una presunta infección reciente por un único arbovirus cuando los resultados son positivos para ese virus mediante una prueba ELISA para IgM, y tienen una infección presunta por flavivirus si el resultado dio positivo para virus del Zika y virus del dengue mediante una prueba ELISA para IgM. El diagnóstico neurológico de los casos de SGB con evidencia de infección arboviral fue confirmado por una revisión de gráficos utilizando los criterios de Colaboración Brighton; un conjunto de criterios de diagnóstico estandarizados de acuerdo con la presentación clínica, los resultados de laboratorio del LCR y los hallazgos electrofisiológicos (6). Las revisiones de gráficos se realizan luego del alta hospitalaria, y >;28 días después de la aparición de signos neurológicos para las personas que siguen hospitalizadas, o mueren.
Se identificaron cincuenta y seis presuntos casos de SGB con aparición de signos neurológicos durante el 1 de enero y el 31 de julio del 2016, incluido un caso antes de la implementación del GBPSS y dos casos identificados durante una evaluación a mitad de año del sistema de vigilancia. Entre los casos presuntos de SGB identificados, 20 pacientes (37%) no tenían evidencia de infección por el virus del Zika, dos (4%) pacientes tenían pendientes los resultados de laboratorio, y 34 (61%) pacientes tenían evidencia de infección por el virus del Zika o por flavivirus. Entre estos 34 pacientes, 10 (18%) tenían infección confirmada por el virus del Zika, 16 (29%) tenían presunta infección por el virus del Zika, y ocho (14%) tenían infección presunta por flavivirus. Además, un (2%) paciente tenía resultados equívocos tanto para el virus del Zika como del dengue mediante ELISA para IgM, y tres (5%) tenían resultados equívocos para el virus de chikunguña mediante ELISA para IgM.
Durante enero y julio del 2016, la media para la cantidad de casos mensuales de personas con presunto SGB y sin evidencias de infección por el virus del Zika o con resultados de laboratorio pendientes, por mes de aparición de signos neurológicos, fue de tres personas (rango = 1-5). En general, el número de personas con presunto SGB y evidencia de infección por el virus del Zika o por flavivirus fue 2.5 veces mayor que el número de personas con presunto SGB y sin evidencia de infección por el virus del Zika, con un número en aumento de los casos que se producen cada mes y que comienzan en abril (figura 1). Los 34 pacientes con presunto SGB y evidencia de infección por el virus del Zika o por flavivirus eran residentes de siete de ocho regiones de salud del Departamento de Salud de Puerto Rico. (figura 2); la media en la edad de estos pacientes fue de 55 años (rango= 21-88 años), y 20 (59%) de los 34 pacientes eran mujeres.
Se han revisado los gráficos para 32 de estos 34 pacientes; se confirmó la presencia de SGB en todos los 32. Se registró enfermedad aguda durante los 2 meses anteriores en los gráficos médicos de 30 (94%) pacientes (Tabla). Los síntomas informados más comúnmente, y asociados a antecedentes de enfermedad aguda fueron sarpullido (n = 18, 53%), fiebre (n = 12, 35%), y diarrea (n = 7, 21%). El intervalo medio entre el antecedente de enfermedad aguda y la aparición de signos neurológicos fue de 5 días (rango= 0–17 días). Todos los 34 pacientes fueron hospitalizados tras la aparición de signos neurológicos, y entre los pacientes a los que se les dio el alta (n = 28) o que han muerto (n = 1) al 18 de agosto, la duración media de la hospitalización fue de 12 días (rango= 6–47 días). Entre los 32 pacientes con revisiones completas de los gráficos, los signos y síntomas clínicos registrados más comúnmente fueron hiporreflexia o arreflexia (n = 31, 97%), debilidad en las piernas (n = 31, 97%), parestesia de piernas (n = 24, 75%), debilidad en los brazos (n = 24, 75%), debilidad facial (n = 20, 63%), adormecimiento de los brazos (n = 19, 59%), y disfagia (n = 19, 59%). Todos los 25 pacientes que fueron sometidos a punciones lumbares tenían disociación citoalbuminológica (concentración aumentada de la proteina en el LCR y una cantidad total de glóbulos blancos en el LCR de <50 células/μl.), lo que suele observarse de manera frecuente en pacientes con SGB. Cinco pacientes tenían pruebas electrofisiológicas, las que indicaron el subtipo de SGB de polineuropatía desmielinizante infalmatoria aguda en los cinco. Todos los 34 pacientes fueron tratados con IVIg. Al 18 de agosto, 21 (62%) de 34 pacientes habían sido ingresados a unidades de terapia intensiva, y 12 (35%) tuvieron que ser asistidos con ventilación mecánica. Al 18 de agosto, cinco (15%) pacientes permanecían hospitalizados, a 15 (44%) se les dio el alta para que regresaran a sus hogares, y a 13 (38%) se los transfirió a rehabilitación o a un centro de enfermería especializada. Un paciente (3%) con presunta infección por flavivirus murió de un choque séptico, a pesar de haber sido tratado con antibióticos de amplio espectro.
Además, se informaron 26 casos de trastornos neurológicos que no eran de SGB al Departamento de Salud de Puerto Rico a través del GBPSS; siete (27%) pacientes tenían evidencia de una infección reciente por el virus del Zika o por flavivirus. Los trastornos neurológicos entre estos siete pacientes incluían tres casos de encefalitis (un paciente tenía infección confirmada por el virus del Zika, uno tenía presunta infección por el virus del Zika, y uno tenía presunta infección por flavivirus); dos casos de mielitis, ambos en pacientes con infección confirmada por el virus del Zika; un caso de déficit neurológico agudo, en un paciente con infección confirmada por el virus del Zika; y un caso de papiledema postinfeccioso, en un paciente con presunta infección por el virus del Zika.
Evaluación del sistema de vigilancia
Durante julio del 2016, se evaluó la exhaustividad del sistema de vigilancia para determinar los presuntos casos de SGB. Se contactaron treinta y dos (46%) de un total de 70 hospitales en la isla. Se les pidió a los integrantes del personal de los departamentos de registros médicos o de control de infecciones que proporcionaran una lista de pacientes que habían sido hospitalizados de enero a junio del 2016, y que tuvieran una Clasificación Internacional de Enfermedad, código para SGB (G61) 10° revisión en su registro médico. Los casos posibles no informados de SGB se definen como pacientes que fueron hospitalizados después de que se dio inicio al GBPSS a mediados de febrero, que tenían estadías hospitalarias de >;3 días, y que no fueron informados al GBPSS. No se incluyeron a los pacientes con diagnóstico final alternativo. Veintiséis (81%) de los 32 hospitales contactados respondieron, incluidos 13 de los 16 hospitales que informaron al menos un caso presunto de SGB y 13 hospitales a partir de una muestra intencional de 16 hospitales seleccionados al azar entre los hospitales restantes en la isla y luego de estratificar por tamaño y región a los hospitales.
Se identificaron dos casos de posible SGB que no habían sido informados de manera directa al GBPSS. Ambos habían enviado espécimenes al Sistema de Vigilancia Pasiva de Enfermedades Arbovirales del Departamento de Salud de Puerto Rico poco tiempo antes de la aparición de la enfermedad neurológica, lo que confirmó la infección por el virus del Zika.;¶; Los pacientes fueron hospitalizados por SGB en mayo y junio respectivamente, y el diagnóstico de SGB fue confirmado mediante la revisión de gráficos.
Discusión
Debido al aumento informado de la incidencia de SGB en países afectados por el virus del Zika (7), el Departamento de Salud de Puerto Rico implementó el GBPSS rápidamente poco después de informar el primer caso de la enfermedad por el virus del Zika (4). Los informes oportunos han permitido la identificación de diez casos de SGB con infección confirmada por el virus del Zika mediante una prueba RT-PCR. Antes de este informe, solo se habían descrito casos individuales de infección confirmada por el virus del Zika en pacientes con SGB (8). Se espera que los casos de SGB con evidencia de infección por flavivirus sean atribuibles al virus del Zika; el flavivirus predominante actualmente en circulación en Puerto Rico; durante el 1 de noviembre del 2015 al 7 de julio del 2016, el Departamento de Salud de Puerto Rico identificó 5 582 casos presuntos de virus del Zika en comparación con solo 136 casos de infecciones por el virus del dengue (5). Aunque las muertes entre los pacientes con SGB son poco frecuentes (1), la gravedad potencial y la carga del SGB sobre el sistema de salud son resaltados por la muerte descrita aquí y por la gran proporción de pacientes que requirieron servicios de terapia intensiva, incluida la ventilación mecánica.
Concuerda con la epidemiología mundial del SGB, la media de la edad de los pacientes con SGB presunto y evidencia de infección por el virus del Zika o por flavivirus fue de >;50 años (9). Si bien el SGB por lo general se da más frecuentemente en hombres que en mujeres (9), la mayoría de los pacientes descritos en este informe eran mujeres. Se planea realizar un análisis para explorar la distribución inesperada de los casos por sexo, incluida la predominancia aparente de mujeres con infección por el virus del Zika en Puerto Rico. Si bien las actividades de asistencia social de los proveedores y la agrupación de casos de SGB podrían explicar parcialmente el aumento en la cantidad de casos mensuales de abril a julio, el incremento en la cantidad de casos concuerda con la transmisión actual del virus del Zika. En la Polinesia Francesa, donde se produjo un brote de la enfermedad por el virus del Zika durante 2013–2014, se informó un incremento en el número de pacientes con SGB (7). A diferencia de la Polinesia Francesa, donde los estudios electrofisiológicos (cuando fueron realizados) identificaron el subtipo de neuropatia axonal motora aguda de SGB (7), en Puerto Rico, el subtipo de SGB de polineuropatía desmielinizante inflamatoria aguda fue identificada en todos los cinco casos de SGB con evidencia de infección por el virus del Zika o por flavivirus que tuvieron estudios electrofisiológicos realizados. Concuerda con otros informes que han hallado una gama de afecciones neurológicas potencialmente asociadas a la infección por el virus del Zika (10), 27% de los 26 pacientes con afecciones neurológicas, distintas del SGB, identificadas mediante el GBPSS tenían evidencia de infección por el virus del Zika o por flavivirus.
Los residentes de Puerto Rico y de países con transmisión actual del virus del Zika y las personas que viajan a estos lugares deben seguir las recomendaciones de prevención de infecciones por el virus del Zika. Dado el incremento potencial en la incidencia de SGB durante la transmisión actual del virus del Zika, los proveedores de atención médica en áreas con transmisión actual a nivel local deben estar familiarizados con las características clínicas del SGB para garantizar el diagnóstico y el tratamiento oportuno del paciente. Los pacientes con signos y síntomas que concuerden con el SGB deben buscar atención médica, sin importar los antecedentes de la enfermedad. Los proveedores de atención médica deben informar los presuntos casos de SGB y otras afecciones neurológicas a las autoridades de salud pública.**
Reconocimientos
Norma Diaz Paris, Juan B. Méndez, Anibal Cruz Sanchez, Jazmín Román, Maria V. Ramos, Zobeida Santiago, Laura Castro, Oficinas Centrales y Regionales de Epidemiología e Investigación, Departamento de Salud de Puerto Rico; Cesar A. Virgen, MD, Universidad de California San Diego; Elba V. Caraballo, PhD, Koralys Torres Alicea, Damaris Laboy Fernández, Janice Perez, MPH, Vera Soltero, JD, MPH, División de Enfermedades Transmitidas por Vectores, CDC; Tyler Chavers, Universidad Emory, Atlanta, Georgia; Yvette Lopez Vazquez, Facultad de Medicina San Juan Bautista, Puerto Rico; Brenda Deliz, MD, Universidad de Puerto Rico; Hospital del Distrito Universitario, Puerto Rico; Hospital Pediátrico Universitario, Puerto Rico; HIMA-San Pablo, Caguas y Bayamón, Puerto Rico; Hospital de la Universidad de Puerto Rico - Dr. Federico Trilla; Hospital Municipal de San Juan, Puerto Rico; Hospital de Auxilios Mutuos, Puerto Rico; Hospital de la Asociación de Veteranos de San Juan, Puerto Rico; Hospital Damas, Puerto Rico; Centro Médico Manatí, Puerto Rico; Centro Médico Mayagüez, Puerto Rico; Hospital del Centro de Médicos, Bayamón y Manatí, Puerto Rico; Centro de Rehabilitación HealthSouth, San Juan, Puerto Rico; Hospital Oriente, Puerto Rico; Hospital Pavia, Arecibo, Santurce, Hato Rey, y Yauco, Puerto Rico; Hospital Ryder Memorial, Puerto Rico.
Autor responsable de la correspondencia: Emilio Dirlikov, GBS@salud.pr.gov, 787-706-4358.
1Oficina de Epidemiología e Investigación, Departamento de Salud de Puerto; 2Servicio de Inteligencia Epidemiológica, División de Educación Científica y Desarrollo Profesional, CDC; 3División de Enfermedades Transmitidas por Vectores, Centro Nacional de Enfermedades Infecciosas Emergentes y Zoonóticas, CDC; 4Oficina de Ayuda Estatal, Tribal, Local y Territorial, CDC; 5Universidad Emory, Atlanta, Georgia; 6Departamento de Neurología y División de Enfermedades Infecciosas, Universidad de Colorado Denver; 7Laboratorio de Emergencias Biológicas y Químicas, Oficina de Preparación y Respuesta de Salud Pública, Departamento de Salud Pública; 8Laboratorio de Salud Pública, Departamento de Salud de Puerto Rico; 9División de Preparación Estatal y Local, Oficina de Preparación y Respuesta de Salud Pública, CDC; 10HIMA-San Pablo, Caguas, Puerto Rico; 11Universidad de Puerto Rico; 12Oficina de Enfermedades Infecciosas, Centro Nacional de Enfermedades Infecciosas Emergentes y Zoonóticas, CDC.
Referencias
- Yuki N, Hartung H-P. Guillain-Barré syndrome. N Engl J Med 2012;366:2294-304. CrossRef PubMed
- Petersen LR, Jamieson DJ, Honein MA. El virus del Zika. N Engl J Med 2016;375:294-5. PubMed
- Thomas DL, Sharp TM, Torres J, et al. Local transmission of Zika virus-Puerto Rico, November 23, 2015-January 28, 2016. MMWR Morb Mortal Wkly Rep 2016;65:154-8. CrossRef PubMed
- Dirlikov E, Ryff KR, Torres-Aponte J, et al. Update: ongoing Zika virus transmission-Puerto Rico, November 1, 2015-April 14, 2016. MMWR Morb Mortal Wkly Rep 2016;65:451-5. CrossRef PubMed
- Adams L, Bello-Pagan M, Lozier M, et al. Update: ongoing Zika virus transmission-Puerto Rico, November 1, 2015-July 7, 2016. MMWR Morb Mortal Wkly Rep 2016;65:774-9. CrossRef PubMed
- Sejvar JJ, Kohl KS, Gidudu J, et al. ; Brighton Collaboration GBS Working Group. Guillain-Barré syndrome and Fisher syndrome: case definitions and guidelines for collection, analysis, and presentation of immunization safety data. Vacuna 2011;29:599-612. CrossRef PubMed
- Cao-Lormeau VM, Blake A, Mons S, et al. Guillain-Barré syndrome outbreak associated with Zika virus infection in French Polynesia: a case-control study. Lancet 2016;387:1531-9. CrossRef PubMed
- Siu R, Bukhari W, Todd A, Gunn W, Huang QS, Timmings P. Acute Zika infection with concurrent onset of Guillain-Barré syndrome. Neurology 2016. Epub July 27, 2016. CrossRef PubMed
- Sejvar JJ, Baughman AL, Wise M, Morgan OW. Population incidence of Guillain-Barré syndrome: a systematic review and meta-analysis. Neuroepidemiology 2011;36:123-33. CrossRef PubMed
- Araujo AQ, Silva MT, Araujo AP. Zika virus-associated neurological disorders: a review. Brain 2016;139:2122-30. CrossRef PubMed
* http://www.cdc.gov/zika/prevention/.
† El formulario para informar los casos de SGB está disponible en español (http://www.salud.gov.pr/Sobre-tu-Salud/Documents/Español.pdf) y en inglés (http://www.salud.gov.pr/Sobre-tu-Salud/Documents/ingl%c3%a9s.pdf).
¶ El Departamento de Salud de Puerto Rico y la División del Dengue de los CDC incorporaron el informe de casos y las pruebas de diagnóstico a sus sistemas actuales de vigilancia del virus del dengue y chikunguña, y además crearon un sistema de vigilancia pasiva de las enfermedades arbovirales en los laboratorios.
** http://www.salud.gov.pr/Sobre-tu-Salud/Pages/ProfesionalesdelaSalud.aspx#gbszika.
 FIGURA 1. Casos informados del síndrome, confirmados o presuntos, de Guillain-Barré (n = 56), por resultado de laboratorio para el virus del Zika y mes de aparición de signos neurológicos - Puerto Rico, del 1 de enero al 31 de julio del 2016
FIGURA 1. Casos informados del síndrome, confirmados o presuntos, de Guillain-Barré (n = 56), por resultado de laboratorio para el virus del Zika y mes de aparición de signos neurológicos - Puerto Rico, del 1 de enero al 31 de julio del 2016
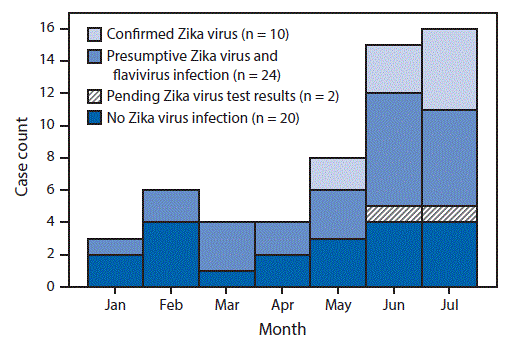
 FIGURA 2. Los casos confirmados y presuntos del Síndrome de Guillain-Barré con evidencia de infección por el virus del Zika o por flavivirus, por región de residencia de salud pública - Puerto Rico, del 1 de enero al 31 de julio del 2016 (N = 34)
FIGURA 2. Los casos confirmados y presuntos del Síndrome de Guillain-Barré con evidencia de infección por el virus del Zika o por flavivirus, por región de residencia de salud pública - Puerto Rico, del 1 de enero al 31 de julio del 2016 (N = 34)
 TABLA. Características, interpretación de los resultados de laboratorio, confirmación del diagnóstico neurológico, y curso de la enfermedad en pacientes con Síndrome de Guillain-Barré (SGB)* y evidencia de infección por el virus del Zika o por flavivirus (N = 34) - Puerto Rico, del 1 de enero al 31 de julio del 2016
TABLA. Características, interpretación de los resultados de laboratorio, confirmación del diagnóstico neurológico, y curso de la enfermedad en pacientes con Síndrome de Guillain-Barré (SGB)* y evidencia de infección por el virus del Zika o por flavivirus (N = 34) - Puerto Rico, del 1 de enero al 31 de julio del 2016
| Características | Media (rango) |
|---|---|
| Edad (años) | 55 (21–88) |
| Sexo | N°. (%) de pacientes |
| Mujer | 20 (59) |
| Interpretación de los resultados de laboratorio | |
| Infección por el virus del Zika confirmada | 10 (29) |
| Presunta infección por el virus del Zika | 16 (47) |
| Presunta infección por flavivirus | 8 (24) |
| Confirmación de diagnóstico neurológico a través de la revisión de gráficos | |
| Pacientes con gráficos revisados | 32 (94) |
| Pacientes con diagnostico confirmado de SGB | 32 (94) |
| Pacientes con revisión de gráficos pendiente | 2 (6) |
| Curso de la enfermedad | |
| Duración (días) (N = 32*) | Media (rango) |
| Aparición de enfermedad de antecedentes agudos a síntomas neurológicos | 5 (0–17) |
| Hospitalización† | 12 (6–47) |
| Enfermedad antecedente (N = 32*) | N°. (%) de pacientes |
| Enfermedad antecedente aguda§ | 30 (94) |
| Sarpullido | 18 (56) |
| Fiebre | 12 (38) |
| Diarrea | 7 (22) |
| Signos y síntomas de enfermedad neurológica (N = 32*) | |
| Hiporreflexia o arreflexia | 31 (97) |
| Debilidad en las piernas | 31 (97) |
| Parestesia de piernas | 24 (75) |
| Debilidad en los brazos | 24 (75) |
| Debilidad facial | 20 (63) |
| Parestesia de brazos | 19 (59) |
| Disfagia | 19 (59) |
| Disociación citoalbuminológica (N = 25)¶ | 25 (100) |
| Hallazgos electrofisiológicos (N = 5)** | |
| Subtipo de polineuropatía desmielienizante inflamatoria aguda | 5 (100) |
| Intervenciones médicas | |
| Ingresados al hospital | 34 (100) |
| Inmunoglobulina G intravenosa | 34 (100) |
| Ingresados a una unidad de terapia intensiva | 21 (62) |
| Asistencia respiratoria mecánica | 12 (35) |
| Resultado clínico (N = 29)† | |
| Dados de alta para que regresen a su casa | 15 (52) |
| Dados de alta y derivados al centro de rehabilitación o centro de enfermería especializada | 13 (45) |
| Muertes | 1 (3) |
* Datos para 32 casos de SGB confirmados que se reunieron mediante la revisión de gráficos del paciente. Debido a que el criterio de revisión de la gráfica, la revisión gráfica está pendiente para dos presuntos casos de SGB con evidencia de infección por el virus del Zika o por flavivirus.
† No incluye los cinco pacientes aún hospitalizados al 18 de agosto del 2016.
§ Se define como enfermedad de antecedente en los dos meses anteriores a la aparición de signos neurológicos, según está registrado en el registro médico.
¶ Se refiere a la concentración de proteína aumentada en el líquido cefalorraquídeo y al conteo total de glóbulos blancos en el líquido cefalorraquídeo <50 células/μl. Se realizaron punciones lumbares y los resultados del líquido cefalorraquídeo estuvieron disponibles para 25 pacientes.
** Estudios electrofisiológicos disponibles para cinco pacientes.
Cita sugerida para este artículo: Dirlikov E, Major CG, Mayshack M, et al. Guillain-Barré Syndrome During Ongoing Zika Virus Transmission - Puerto Rico, January 1-July 31, 2016. Informe Semanal de Morbilidad y Mortalidad (MMWR) 2016;65:910–914. DOI: http://dx.doi.org/10.16/mmwr.mm6534e1.
El uso de nombres de marcas y fuentes comerciales se utiliza solamente para efectos de identificación y no constituye aval alguno por parte del Departamento de Salud y Servicios Humanos de los EE. UU.
Las referencias de sitios en Internet que no son de los CDC se ofrecen como un servicio a los lectores del MMWR y no constituyen ni implican el aval de estas organizaciones o sus programas por parte de los CDC o del Departamento de Salud y Servicios Humanos de los EE. UU. Los CDC no son responsables por el contenido de las páginas de estos sitios. Las direcciones URL enumeradas en el MMWR estaban actualizadas hasta la fecha de la publicación.
Todas las versiones HTML de los artículos del MMWR son generadas de pruebas finales a través de procesos automatizados. Esta conversión podría resultar en la traducción de caracteres o errores de formato en la versión HTML. Los usuarios deben remitirse a la versión en PDF (https://www.cdc.gov/mmwr) o a la copia original en papel del MMWR para obtener versiones para imprimir del texto, las cifras y las tablas oficiales.
Las preguntas o mensajes con respecto a errores en el formato deben dirigirse a mmwrq@cdc.gov.
Ayuda con los formatos de archivos:
¿Cómo se visualizan los diferentes formatos de archivos (PDF, DOC, PPT, MPEG) en este sitio?- Esta página fue revisada el 29 de agosto de 2017
- Esta página fue modificada el 29 de agosto de 2017
- Fuente del contenido:


 CompartirCompartir
CompartirCompartir